REAKSI SUBTITUSI DAN REAKSI ELIMINASI PADA SENYAWA ORGANIK
REAKSI SUBTITUSI DAN
REAKSI ELIMINASI PADA SENYAWA ORGANIK
Dalam
kimia organik, banyak reaksi yang dapat terjadi yang melibatkanikatan
kovalen di antara atom karbon dan heteroatom lainnya
seperti oksigen,nitrogen,
atau atom-atom halogen lainnya. Beberapa reaksi dalam kimia organic diantaranya:
1. Reaksi Subtitusi è adalah reaksi penggantian (penukaran) suatu gugus
atom oleh gugus atom lain. Pada reaksi subtitusi tidak terjadi perubahan
ikatan, ikatan tunggal –> ikatan tunggal.
Contoh
:
a) Reaksi
monoklorinasi propana (pengantian satu atom H oleh satu atom Cl), misalnya: C3H8 +
Cl2 –> C3H7Cl + HCl
b) Reaksi
dibrominasi propana (penggantian dua atom H oleh dua atom Br), misalnya : C3H8 +
2Br2 –> C3H6Br2 + 2HBr.
Macam-macam reaksi
subtitusi, diantaranya:
| 1) Reaksi substitusi nukleofilik. Pada reaksi substitusi nukleofilik atom/ gugus yang diganti mempunyai elektronegativitas lebih besar dari atom C, dan atom/gugus pengganti adalah suatu nukleofil, baik nukleofil netral atau nukleofil yang bermuatan negatif. |
2) Reaksi
substitusi elektrofilik. Benzena memiliki rumus molekul C6H6,
dari rumus molekul tersebut benzena termasuk golongan senyawa hidrokarbon tidak
jenuh. Namun ternyata benzena mempunyai sifat kimia yang berbeda dengan senyawa
hidrokarbon tidak jenuh. Beberapa perbedaan sifat benzena dengan senyawa
hidrokarbon tidak jenuh adalah diantaranya bahwa benzena tidak mengalami reaksi
adisi melainkan mengalami reaksi substitusi. Pada umumnya reaksi yang terjadi
terhadap molekul benzena adalah reaksi substitusi elektrofilik, hal ini
disebabkan karena benzena merupakan molekul yang kaya electron.
Ada
4 macam reaksi substitusi elektrofilik terhadap senyawa aromatik,yaitu: |
2. Reaksi Eliminasi adalah reaksi penghilangan suatu gugus atom pada suatu senyawa. Pada reaksi elimiasi teradi perubahan ikatan, ikatan tunggal => ikatan rangkap. Dalam reaksi ini terjadi penghilangan 2 atom atau gugus untuk membentuk ikatan rangkap atau struktur siklis. Kebanyakan reaksi eliminasi menyangkut kehilangan atom bukan karbon. Reaksi eliminasi secara umum :
Contoh
:
CH3–CH3 –>
CH2=CH2 + H2
CH3–CH2Br
–> CH2=CH2 + HBr
CH3–CH2OH
–> CH2=CH2 + H2O
Reaksi satu langkah disebut dengan reaksi E2.
Sedangkan reaksi dua langkah disebut dengan reaksi E1. Harap diingat bahwa
symbol angka pada huruf e (yang berarti elimination) tidak melambangkan jumlah
langkah. E2 dan E1 menyatakan kinetika reaksi, yaitu berturut-turut bimolekuler
dan unimolekuler.
a) Reaksi
E1
Reaksi
E1 adalah reaksi eliminasi dimana suatu karbokation (suatu zat antara yang tak
stabil dan berenergi tinggi, yang dengan segera bereaksi lebih lanjut) dapat
memberikan sebuah proton kepada suatu basa dan menghasilkan sebuah alkena. Pada
reaksi SN1, salah satu cara karbokation mencapai produk yang stabil
ialah dengan bereaksi dengan sebuah nukleofil.
Karbokation
adalah suatu zat antara yang tak stabil dan berenergi tinggi. Karbokation
memberikan kepada basa sebuah proton dalam reaksi eliminasi, dalam hal ini
reaksi E1 menjadi sebuah alkena.
Ø Mekanisme
E1
·
Tahap 1 (lambat)
Pertama
dalam reaksi eliminasi adalah tahap lambat dan merupakan tahap penentu laju
dari reaksi keseluruhan. Suatu reaksi E1 yang khas menunjukkan kinetika
order-pertama, dengan laju reaksi hanya bergantung pada konsentrasi alkil
halide saja.
·
Tahap 2 (cepat)
Dalam
tahap dua reaksi eliminasi, basa itu merebut sebuah proton dari sebuah atom
karbon yang terletak berdampingan dengan karbon positif. Elektron ikatan sigma
karbon hidrogen bergeser ke arah muatan positif, karbon itu mengalami Rehibridisasi
dari keadaan sp3 ke keadaan sp2, dan
terbentuklah alkena.
Karena suatu reaksi E1 berlangsung lewat zat antara
karbokation, maka tidak mengherankan bahwa alkil halida tersier lebih cepat daripada
alkil halida lain. |
b) Reaksi
E2
Reaksi
E2 (eliminasi bimolekular) ialah reaksi eliminasi alkil halida yang paling
berguna. Reaksi E2 alkil halida cenderung dominan bila digunakan basa kuat,
seperti –OH dan –OR, dan temperatur tinggi. Secara khas reaksi E2
dilaksanakan dengan memanaskan alkil halida dengan K+ -OH / Na+ -OCH2CH3 dalam
etanol.
Reaksi
E2 berjalan tidak lewat suatu karbokation sebagai zat-antara, melainkan berupareaksi
serempak (concerted reaction) yakni terjadi pada satu tahap, sama seperti
reaksi SN2.
ü Basa
membentuk ikatan dengan hydrogen
ü Elektron-elektron
C-H membentuk ikatan pi
ü Brom
bersama sepasang elektronnya meninggalkan ikatan sigma C-Br.
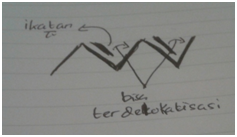
Perhatikan
gambar berikut :
Persamaan
diatas menunjukkan mekanisme, dengan anak panah bengkok menyatakan “pendorongan
elektron” (electron-pushing). Dalam reaksi E2, seperti dalam reaksi E1,
alkil halida tersier bereaksi paling cepat dan alkil halida primer paling
lambat. (Bila diolah dengan suatu basa, alkil halide primer biasanya begitu
mudah bereaksi substitusi, sehingga sedikit alkena terbentuk).
Perbedaan
antara mekanisme eliminasi E1 dan E2.
E1
a) membentuk
karbokation
b) karbokation
memberi proton pada basa lalu terbentuk alkena
c) basa
merebut proton dari atom C (beta, C yang berdampingan dengan C+)
E2
a) nukleofil
langsung mengambil proton dari atom C (beta) pada atom C gugus pergi
b) tidak
terjadi pembentukan karbokation
c) pembentukan
secara serempak
Perbandingan
E1 dan E2.
E1
terjadi pada:
terjadi pada:
a) konsentrasi
basa rendah
b) dengan
pelarut basa
c) dengan
substrat tersier dan beresonansi (alkil halida)
E2
terjadi pada:
terjadi pada:
a) pada
basa kuat dengan konsentrasi tinggi
o Alkil
halida+basa kuat+panas è E2
o Alkil
halida+asam kuat+panas è E1
o Alkohol+asam
kuat+panas è E1










seperti dalam reaksi E1, alkil halida tersier bereaksi paling cepat dan alkil halida primer paling lambat. Apakah yang mempengaruhinya dan berikan contoh alkilhalida tersier dan alkil halida primer.
BalasHapusAlkil halida tersier (3o): Tiga karbon terikat pada karbon C-X. Itulah yang menyebabkan alkil halida tersier lebih reaktif. Sedangkan Alkil halida primer (1o): Sebuah karbon yang terikat pada karbon C-X.
HapusContoh alkil halida tersier.
CH3
|
H3C – C – X
|
CH3
Contoh alkil halida primer.
CH3CH2 – CH2X
Benzena memiliki rumus molekul C6H6, dari rumus molekul tersebut benzena termasuk golongan senyawa hidrokarbon tidak jenuh. Namun ternyata benzena mempunyai sifat kimia yang berbeda dengan senyawa hidrokarbon tidak jenuh. jelaskan kenapa hal tersebut bisa terjadi ?
BalasHapusJelaskan jenis2 reaksi substitusi berserta contoh nya
BalasHapusJenis jenis reaksi subtitusi antara lain:
Hapus1. Reaksi Substitusi Radikal Bebas.
Reaksi substitusi radikal bebas terjadi apabila gugus yang mengganti adalah radikal bebas. Pereaksi radikal bebas adalah atom atau gugus atom yang mengandung sebuah elektron yang tidak berpasangan. Contohnya adalah reaksi antara metana dengan gas klor mengasilkan monoklor-metana dan asam klorida.
2. Reaksi Substitusi Nukleofilik.
Reaksi substitusi nukleofilik terjadi apabila gugus yang mengganti merupakan pereaksi nukleofil. Contoh reaksi substitusi nukleofilik adalah reaksi antara etanol dengan asam bromida menghasilkan etil-bromida.
3. Reaksi substitusi elektrofilik.
Reaksi substitusi nukleofilik terjadi apabila gugus yang mengganti merupakan pereaksi elektrofil. Reaksi substitusi elektrofilik biasanya terjadi ada senyawa aromatic, disebut dengan reaksi substitusi elektrofilik aromatic. Benzene lebih mudah melangsungkn reaksi substitusi elektrofilik daripada nukleofilik.
Terima kasih
adakah sifat khusus dari alkil halida tersier dan alkil halida primer?
BalasHapusTidak ada. Hanya saja pada alkil halida tersier memiliki kemampuan untuk mengikat tiga atom C yang lain. Sedangkan alkil halida primer hanya mampu mengikat satu atom C yang lain.
HapusTerima kasih
Assalamualaikum, bisakah anda jelaskan perbedaan antara substitusi dengan eliminasi? terima kasih
BalasHapusTerima kasih atas pertanyaannya saudara wahyu. Saya akan mencoba menjawab pertanyaan anda. Reaksi substitusi adalah suatu reaksi penggantian gugus fungsional pada senyawa kimia tertentu dengan gugus fungsional yang lain. Sedangkan reaksi eliminasi adalah suatu jenis reaksi organik dimana dua substituen dilepaskan dari sebuah molekul baik dalam satu atau dua langkah mekanisme.
HapusAssalamualaikum,,,
BalasHapusBagaimana reaksi eliminasi dari 1 metil,1 propanol?
Assalamualaikum,,,
BalasHapusBagaimana reaksi eliminasi dari 1 metil,1 propanol?
Jika senyawa propana mengalami reaksi eliminasi menghasilkan?
BalasHapusKalau reaksi eliminasi dari C3H8 berapa ya?
BalasHapus